cho 20,85g hh gồm Al ,Fe có ti lệ mol tương ứng là 1:2 vào dd H2SO4 loãng thì thu đc V lit khí ở đktc.V=?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
► Đặt nAl = x; nFe = y ⇒ nNa = 2x ||⇒ Al tan hết ⇒ Y chỉ có Fe.
Bảo toàn electron: nNa + 3nAl = 2nH2 ⇒ 2x + 3.x = 2 × 2 ⇒ x = 0,8 mol.
nFe = nH2 = 0,5 mol ||► nFe : nAl = 0,5 : 0,8 = 5 : 8

Đáp án B
► Đặt nAl = x; nFe = y ⇒ nNa = 2x ||⇒ Al tan hết ⇒ Y chỉ có Fe.
Bảo toàn electron: nNa + 3nAl = 2nH2 ⇒ 2x + 3.x = 2 × 2 ⇒ x = 0,8 mol.
nFe = nH2 = 0,5 mol ||► nFe : nAl = 0,5 : 0,8 = 5 : 8

Đáp án B
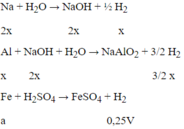
Ta có : a = 0,25V;
còn : x + 3x/2 = 5x/2 = 2,5x = V suy ra x = V/2,5
Vậy a/x = 0,25V/ 0,4V = 5/8

Đáp án B
Giả sử số mol Al là x thì số mol Na là 1,25x.
Cho X tác dụng với H2O thì số mol H2 thu được là 2,125x mol.
Z tác dụng với H2SO4 loãng thu được 0,25V lít khí tức 0,53125x mol.
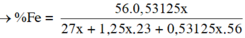
= 74,795 %

Đáp án : D
Na + H2O -> NaOH + 1 2 H2
NaOH + Al + H2O -> NaAlO2 + 3 2 H2
Vì nNa > nAl => chất rắn chỉ còn Fe
⇒ n F e = n H 2 s a u = 0 , 25 V 22 , 4 ( m o l )
⇒ n H 2 = 1 2 n N a + 3 2 n A l = V 22 , 4
Mà nAl : nNa = 4 : 5
=> nAl = 8V/(17.22,4) ; nNa = 10V/(17.22,4)
=> %mFe = 34,80%

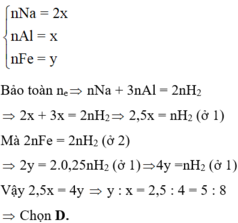
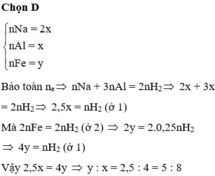
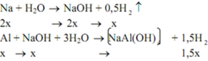
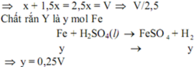


\(n_{Al}=a;n_{Fe}=b\\ n_{Al}:n_{Fe}=1:2\\ \Leftrightarrow2n_{Al}=n_{Fe}\\ \Leftrightarrow2n_{Al}-n_{Fe}=0\\ \Rightarrow\left\{{}\begin{matrix}27a+56b=20,85\\2a-b=0\end{matrix}\right.\\ \Rightarrow a=0,15;b=0,3\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Fe++H_2SO_4\rightarrow FeSO_4+H_2\\ n_{H_2}=0,15\cdot\dfrac{3}{2}+0,3=0,525mol\\ V_{H_2}=11,76l\)